Les bactéries résistent toujours davantage aux remèdes, les antibiotiques. A tel point que certaines sont en passe de devenir intraitables. Au-delà de la nécessaire sensibilisation des médecins, des vétérinaires et du grand public au mésusage de ces médicaments, des solutions sont à l’étude dans des laboratoires. La bataille contre ces ennemis invisibles s’annonce complexe.
Quel cachotier le ticagrelor ! Ce médicament prescrit contre les maladies coronaires possède une vertu jusqu’ici insoupçonnée. Il est capable de tuer les microbes les plus pathogènes, indifférents aux antibiotiques classiques, tels que Staphylococcus aureus et Staphylococcus epidermidis, résistants à la méthicilline, et Enterococcus faecalis, résistant à la vancomycine. A l’origine de cette découverte fortuite, l’équipe de Cécile Oury et Patrizio Lancellotti, de l’ULiège, espère bien en profiter pour concevoir un nouveau traitement efficace contre des superbactéries.
Tous les bénéfices des antibiotiques risquent d’être anéantis.
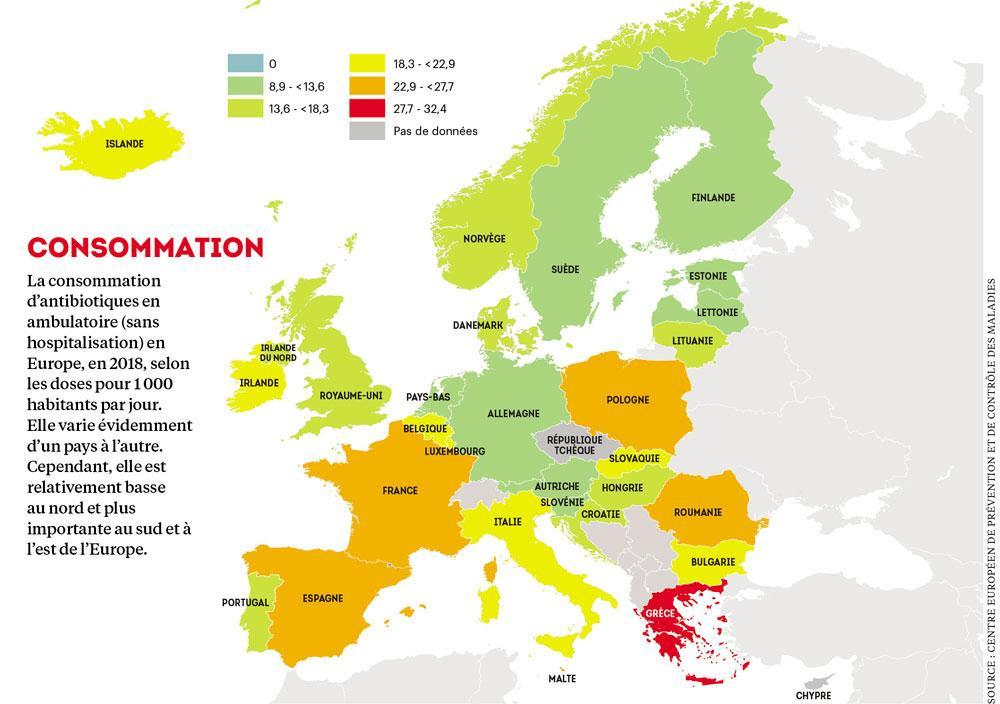
Pour comprendre l’importance de la découverte, il faut rappeler que ces staphylocoques peuvent entraîner des infections nosocomiales, des maladies graves, voire la mort. Quant aux entérocoques résistants à la vancomycine, ils figurent à la quatrième place sur la liste des bactéries les plus menaçantes pour la santé humaine, selon l’Organisation mondiale de la santé (OMS), et pour lesquelles il est urgent d’avoir de nouveaux antibiotiques. En d’autres termes, c’est un peu comme si ces scientifiques liégeois avaient découvert un nouveau gisement de pétrole. Car les raisons d’inquiétude sont bien avérées. Les chiffres donnent le vertige et tous vont dans le même sens pour dresser un constat alarmant. Ainsi, en 2017, une étude du Centre fédéral d’expertise des soins de santé concluait à un véritable scénario catastrophe, celui où » tous les bénéfices des antibiotiques risquent d’être anéantis « . Chaque année, 530 décès en Belgique sont déjà imputables à la résistance antimicrobienne. La Belgique figure d’ailleurs parmi les Etats européens où la consommation de ces molécules demeure trop élevée. En 2018, elle était le septième plus gros prescripteur européen d’antibiotiques en ambulatoire (sans hospitalisation), précédée par la Grèce, la Roumanie, l’Espagne, la France, la Pologne et l’Irlande. Soit un usage environ 2,5 fois plus élevé que celui des Pays-Bas, un modèle en la matière. Voilà pour les chiffres, qu’on pourrait multiplier. Ceux, par exemple, de l’OMS, évoquent » un tsunami au ralenti » : si rien n’est fait, les bactéries résistantes aux antibiotiques tueraient jusqu’à dix millions de personnes par an en 2050, dans le monde, soit plus que le cancer. Ou encore les prévisions de l’OCDE (Organisation de coopération et de développement économiques), qui prédisent qu’entre 2015 et 2050, ce problème causerait dans l’Union européenne 33 000 décès par an.
» Malgré des alarmes tirées à répétition depuis dix ans, une guerre des tranchées semble inévitable, commente Yves Van Laethem, spécialiste en maladies infectieuses au CHU Saint-Pierre, à Bruxelles. Il n’existe aucune terre de « virginité » et, partout dans le monde, le taux d’antibiorésistance progresse. » Aucun spécialiste n’en doute plus, les impasses thérapeutiques anti-infectieuses sont inéluctables et surviendront plus fréquemment. Elles peuvent frapper n’importe qui, à n’importe quel âge, dans n’importe quel pays.
On parle de résistance lorsqu’une bactérie n’est plus mise hors de combat par un médicament auquel elle était jusqu’ici sensible. Au départ, il s’agit d’un phénomène naturel : les organismes vivants que sont les bactéries, mais aussi les virus ou les champignons, développent des mécanismes de survie face aux médicaments destinés à les éliminer. Les souches bactériennes résistantes aux antibiotiques acquièrent ainsi un avantage sur celles qui ne le sont pas. Il en va de même pour les virus face aux antiviraux et pour les champignons face aux antifongiques.
Mais si le phénomène est inéluctable, il n’en est pas moins grandement accéléré par le mauvais usage des médicaments tant chez l’homme que chez l’animal. Les prescriptions inappropriées d’antibiotiques, les interruptions intempestives du traitement dès les premiers signes d’amélioration, pour ce qui est de la médecine humaine, et, en médecine vétérinaire, l’utilisation préventive excessive d’antibiotiques ont accéléré l’apparition de résistances. Car l’existence de souches bactériennes résistantes chez des animaux avec lesquels l’homme est en contact ou présents dans la chaîne alimentaire peut être une voie de transmission de l’antibiorésistance. Aujourd’hui, en Europe, 50 % de la production d’antibiotiques – les mêmes que ceux administrés aux humains – sont destinés à l’élevage.
Les bactéries s’accrochent également aux valises des touristes, circulant à toute vitesse avec la mondialisation. La moitié des touristes revenus de séjours en zones tropicales, notamment ceux qui y ont pris des antibiotiques, sont porteurs d’entérobactéries multirésistantes, y compris aux traitements les plus récents.

Le déclic : NDM-1 et MCR-1
L’exemple de la NDM-1 éclaire parfaitement les dangers d’un monde postantibiotiques. Elle fait désormais figure, avec d’autres, de superbactérie. Identifiée pour la première fois en Inde, en 2009, la New Delhi métallo-bêta-lactamase s’est depuis répandue partout, au Royaume-Uni, en Irlande en Grèce… et jusqu’en Belgique. L’Italie, par exemple, connaît actuellement une hausse significative des cas d’infection à cet agent pathogène, responsable de la dysenterie mais aussi du choléra.
La NDM-1 fonctionne sur un principe assez simple. En fait, des classes d’antibiotiques tirent leur efficacité d’une particularité de leur structure chimique, le noyau bêta-lactame : il empêche la fabrication de la paroi cellulaire d’une bactérie qui se reproduit. Mais la fameuse NDM-1 a trouvé la parade. Grâce au zinc qu’elle contient, elle parvient à briser le noyau bêta-lactame et à rendre la molécule d’antibiotique inopérante, même celles de dernier recours, tels que les carbapénèmes, qu’il s’agit donc de préserver le plus longtemps possible des résistances qui ont commencé à apparaître.
En 2016, une seconde épreuve a été vécue comme un véritable choc : l’apparition de résistances à la colistine, un vieil antibiotique de dernier recours également, utilisé en médecine humaine et en médecine vétérinaire (et d’abord chez les porcs et les poulets). Un choc, parce que jusqu’ici, les résistances connues étaient liées à un gène mutant porté par un chromosome bactérien, donc pas échangeable entre bactéries. Au contraire, dans le cas présent, le gène baptisé MCR-1 se trouve sur un plasmide, une molécule d’ADN circulaire, qui peut être transféré à une autre bactérie, qui deviendra à son tour résistante. En clair, les bactéries ont acquis un panel de connaissances si extraordinaire qu’elles sont désormais capables de se transmettre la résistance entre elles.
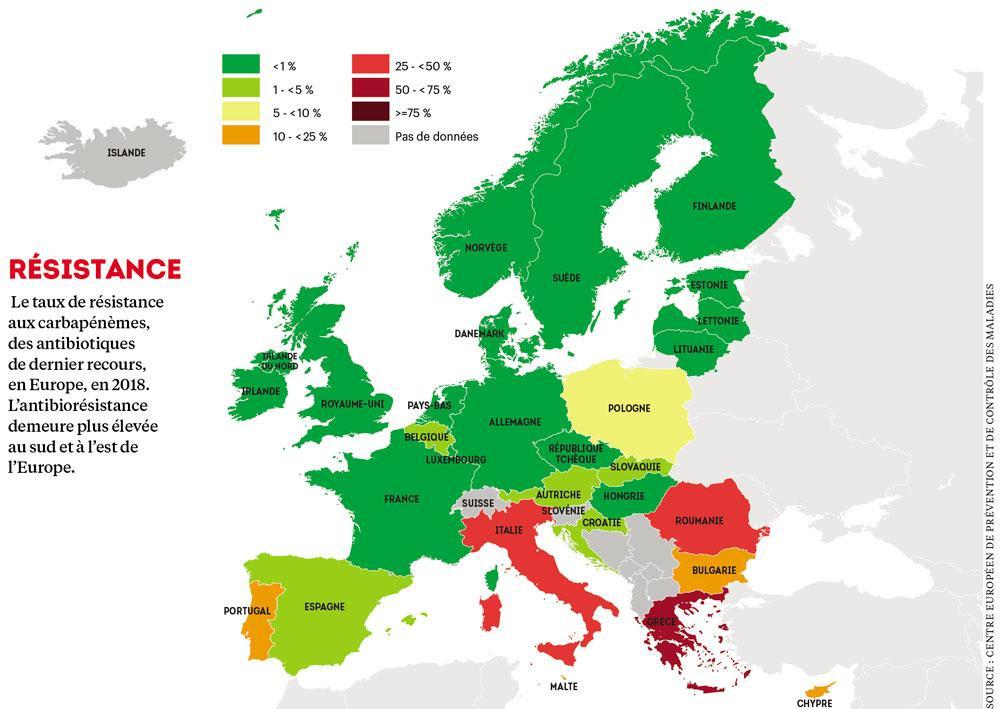
Ces épisodes ne sont qu’un exemple de cette résistance en émergence partout au monde. Très récemment, l’OMS a dressé, pour la première fois, une liste des agents pathogènes prioritaires résistants aux antibiotiques. Au sommet de ce palmarès se retrouvent des bactéries hospitalières comme les entérobactéries productrices de carbapénémases menant le vie dure aux carbapénèmes ( voir ci-dessus). Ensuite, des bactéries trouvées dans les sols ou dans la nourriture, comme la salmonelle. La gonorrhée et la tuberculose sont devenues aussi très préoccupantes. Tôt ou tard, elles parviendront à déjouer toutes les thérapies.
Pourtant, face à ces ennemis invisibles, des initiatives ont été entreprises, en particulier dans le secteur hospitalier et avec un certain succès. La Belgique fut ainsi la première à mettre en place une commission de coordination de la politique en matière d’antibiotiques (Bapcoc), une originalité alors en Europe. Mais plus aucun progrès n’a été enregistré ces dernières années en médecine humaine et la consommation ne diminue plus. Les médecins généralistes continuent d’être pointés du doigt, eux qui, dans leur pratique, se trouvent très rarement confrontés à l’évidence du phénomène de résistance. Difficile, dès lors, de les convaincre de réduire leurs ordonnances. Sans compter la multiplication des génériques, dont l’effet a facilité les prescriptions et entraîné une forte diminution du prix des antibiotiques.
Du côté de la médecine animale, l’utilisation des antibiotiques a, elle, baissé. Voici cinq ans, le secteur s’est accordé sur un code de bonne conduite. » Il y a eu, c’est vrai, une prise de conscience « , reconnaît Marius Gilbert, chercheur en épidémiologie au sein de la faculté des sciences de l’ULB. Le plan a engendré une diminution de l’usage des antibiotiques dits » critiques » (céphalosporines de 3e et 4e générations et fluoroquinolones) de 79,1 % depuis 2011 (année de référence) et de 69,8 % des aliments médicamenteux avec antibiotiques. Enfin, les antibiotiques ne sont plus en » open bar « . Des règles obligent les vétérinaires à faire des antibiogrammes avant de prescrire des antibiotiques. » Les résultats sont là et l’évolution s’avère durable « , commente Fabiana Dal Pozzo, coordinatrice à l’Amcra, qui rassemble tous les acteurs impliqués, de l’éleveur à l’Agence du médicament. Les données se révèlent, en revanche, moins bonnes concernant la réduction de l’utilisation totale d’antibiotiques avant 2020 : l’objectif était de 50 %, il stagne à 35,4 % depuis 2011.

Pour autant, la Belgique reste une élève plutôt moyenne en Europe. En 2016, elle figurait à la cinquième place des plus gros utilisateurs d’antibiotiques, derrière Chypre, l’Espagne, l’Italie et la Hongrie. En réalité, la situation n’est guère encourageante. En Asie, en Inde, en Afrique, la consommation de viande augmente drastiquement. Cette hausse s’accompagne d’une expansion de l’élevage intensif, dans lequel les antimicrobiens sont utilisés en routine pour maintenir la productivité et la santé des élevages. Résultat : les résistances des infections aux antibiotiques croissent dans ces pays émergents. » L’accès aux antibiotiques à usage vétérinaire y est moins régulé. C’est très préoccupant, car ces gènes de résistance voyagent. On sait qu’on peut les retrouver très loin de leur pays d’origine « , poursuit Marius Gilbert. Conséquence : » Les efforts faits dans une partie du monde peuvent s’avérer vains si l’antibiorésistance augmente considérablement ailleurs. »
Le concert des mises en garde finit quand même par devenir audible, voire assourdissant. Des experts ont longtemps plaidé pour la mise en place d’une » task force « , copiée sur le modèle de l’OMS : » One world, one health » (NDLR : un monde, une santé). » Le principe repose sur l’idée que le problème est global : les antibiorésistances ne se transmettent pas uniquement entre hommes mais aussi par les animaux et l’environnement, explique Martine Delanoy, conseillère stratégique au SPF Santé publique. Il faut donc faire coopérer tous les secteurs et tous les niveaux. »

En Belgique, le concept » One health » est… plutôt naissant et un plan d’attaque est en cours de finalisation. Ce 22 novembre, en effet, un avant-projet de ce plan sera soumis aux pouvoirs publics, professions médicales, industrie pharmaceutique et alimentaire. Il proposera (enfin) des objectifs chiffrés et quantifiables. Si elle se veut efficace, la réponse apportée ne peut qu’être collective. » C’est très comparable à la question du réchauffement climatique « , avance le professeur Van Laethem. Ça doit être une prise de conscience mondiale. » Car, selon lui, » les bactéries sont clairement en train de gagner la bataille « . Dès lors, il ne faut fermer aucune porte et attaquer sous tous les angles. Des solutions sont à l’étude dans les laboratoires. Les voici.

Stratégie 1 : élargir l’arsenal
Utiliser sans cesse les mêmes antibiotiques augmente la probabilité de faire émerger des bactéries qui leur sont résistantes. Il faut donc trouver de nouvelles recrues. Or, jusqu’à très récemment, c’était un domaine que de nombreux laboratoires pharmaceutiques avaient abandonné. Aucune classe d’antibiotiques vraiment originale n’a été découverte en vingt-cinq ans et les molécules dites nouvelles n’étaient que de très proches cousines de celles dont les brevets arrivaient à expiration. Les raisons ? Convaincre les firmes de s’engager dans la recherche est une tâche difficile puisqu’il s’agit de développer des médicaments dont l’usage sera par définition restreint afin d’éviter l’acquisition de résistance à ces nouveaux antibiotiques. En clair, l’oncologie, la maladie d’Alzheimer ou le cholestérol sont infiniment plus rentables. Depuis peu, » on sent un frémissement chez les industriels et des start-up tentent de relever le défi « , d’après Yves Van Laethem.
La plupart de nos antibiotiques ont été découverts dans les années 1940 à 1960, » l’âge d’or des antibiotiques « . Les scientifiques venaient alors de se rendre compte que des bactéries du sol sécrétaient des substances qui tuaient d’autres bactéries, les antibiotiques. Les compagnies pharmaceutiques se sont alors mises à cribler les sols de la planète. Dans les sols de la jungle de Bornéo, ils ont trouvé la vancomycine. Au pied du mont Ararat, en Turquie, la daptomycine, et l’érythromycine sur une île des Philippines. Puis, c’est devenu plus difficile. En fouillant les sols, on retrouvait toujours et encore les mêmes substances. Ils se sont alors tournés vers la chimie synthétique en espérant pouvoir créer de nouvelles molécules. Sans succès. On observe à présent un important retour vers la nature. Des chercheurs prospectent les océans, le pergélisol, la cime des arbres, explorent des grottes profondes à la recherche de nouveaux antibiotiques. Mais il n’y a pas encore eu de révolution.
En Europe, 50 % de la production d’antibiotiques sont destinés à l’élevage.
D’autres pistes seraient plus prometteuses. Plutôt que de simplement identifier des molécules qui tuent les bactéries, certains chercheurs essaient de comprendre comment elles tuent, pourquoi elles mutent, se disséminent et résistent. En décortiquant ces mécanismes, on identifie précisément des cibles qui pourront interagir avec les antibiotiques. Il est également question de travailler sur des combinaisons de plusieurs antibiotiques, ou d’un antibiotique avec un adjuvant, qui devraient permettre aux traitements de gagner en efficacité.
D’où une autre éventuelle mesure : ne plus prescrire d’antibiotiques sans diagnostic préalable. En médecine humaine, la prescription d’antibiotiques est le plus souvent effectuée sans recourir en amont à un diagnostic pour confirmer la présence d’une infection bactérienne et d’une éventuelle résistance (c’est-à-dire savoir à quels antibiotiques la bactérie peut résister). Une voie pour améliorer leur usage repose sur des tests diagnostiques précoces et efficaces. Autrement dit, correctement cibler dès le début de l’infection plutôt qu’utiliser par simplicité des antibiotiques dits à spectre large, des bombes à retardement car ils vont induire très vite un renforcement de la bactérie. Des tests rapides de diagnostic de la résistance arrivent. Plusieurs groupes de recherche en Belgique s’appliquent à mettre au point ce type de tests.

Stratégie 2 : la vaccination
D’autres chercheurs travaillent sur des vaccins. En effet, il est scientifiquement démontré que les vaccins réduisent l’usage des antibiotiques, en diminuant la fréquence de certaines infections, donc des traitements anti-infectieux, donc de la pression sélective de résistance. Ainsi, par exemple, les infections causées par la bactérie Streptococcus pneumoniae. Le vaccin contre le pneumocoque a permis de réduire de 50 % l’administration d’antibiotiques.
Dans ce même élan, face aux staphylocoques, premiers agents responsable d’infections nosocomiales et dont de nombreuses souches sont multirésistantes, laissant entrevoir des impasses thérapeutiques, on mise aussi sur le développement de vaccins. Reste que ces pistes demeurent des solutions à court terme, selon les experts interrogés. D’abord, parce que les vaccins antipneumocoque forment des » barrages » et qu’ils ne sont pas » efficaces à 100 % « . Ensuite, parce que » la mise au point d’un vaccin contre les staphylocoques reste lointaine « .
Mais les stratégies précédentes ne constituent pas à proprement parler des alternatives aux antibiotiques, mais plutôt des moyens d’optimiser leur usage. Et, surtout, elles ne suffiront pas. » Des alternatives ? Oui, il y en a de crédibles « , relève Yves Van Laethem. Parmi lesquelles celles-ci.

Stratégie 3 : les anticorps monoclonaux anti-infectieux
Contrairement aux antibiotiques, les anticorps monoclonaux anti-infectieux bloquent les facteurs de virulence des bactéries sans les détruire. Ces protéines complexes attaquent, sur le modèle du système immunitaire lui-même, les mécanismes pathologiques (virus, bactéries, parasites, cellules altérées ou tumorales de l’organisme) à l’origine de la production d’antigènes chez le malade. Il s’agit, en gros, de désarmer la bactérie qui reste présente mais plus capable d’être infectieuse. On connaît leur mécanisme d’action. A ce jour, la plupart des anticorps monoclonaux sont développés pour lutter contre des cancers. Issus des biotechnologies, ils présentent plusieurs avantages : thérapie ciblée, moindre susceptibilité de résistance et pas de dommages sur le microbiote. Enfin, une seule injection peut suffire, comparativement aux doses journalières d’antibiotiques qui sont, la plupart du temps, nécessaires. De fait, comme les anticorps monoclonaux déjà utilisés en cancérologie ou contre certaines maladie autoimmunes, ces traitements s’administrent par voie intraveineuse. Et comme les anticorps produits par notre propre organisme, ces molécules thérapeutiques persistent longtemps dans l’organisme avant d’être éliminées, offrant une protection de plusieurs mois. » Quelques anticorps monoclonaux anti-infectieux sont déjà sur le marché, notamment contre le Clostridium difficile « , enchaîne le médecin. Cette bactérie occupe toute la place de la flore. Elle peut entraîner des diarrhées, parfois des pertes de sang. Dans de rares cas, elle peut entraîner une dilatation et une perforation de l’intestin et, exceptionnellement, le décès. Concrètement, le traitement neutralise deux toxines produites par la bactérie. Il a, en tout, cas, fait chuter son taux de récurrence, ce qui pourrait permettre de mieux contrôler sa présence dans les milieux hospitaliers.
D’autres anticorps monoclonaux sont en cours de tests, notamment contre Escherichia coli ou Klebsiella pneumoniae. » Au rythme actuel, il n’est pas exclu que certains de ces traitements arrivent sur le marché dans les cinq prochaines années. » Il faut cependant relativiser. La complexité de production se répercute logiquement sur le coût des traitements, de l’ordre de dizaines de milliers d’euros par an et par personne.

Stratégie 4 : les phages, ces virus mangeurs de bactéries
Tout aussi spécifiques que les anticorps monoclonaux, les phages sont des micro-organismes présents dans la nature. Ces espèces de virus choisissent leur cible, une bactérie en l’occurrence, dans laquelle ils injectent leur ADN pour s’y multiplier, former une armée et détruire leur hôte. En résumé, ils viennent se coller à la bactérie et la tuent de l’intérieur. » C’est une arme spécifique et écologique « , signale Yves Van Laethem. Dit autrement, il s’agit d’une thérapie ciblée, à l’image d’un anticorps monoclonal, qui ne détruit que la bactérie visée.
Etonnament, les pays de l’Est, Géorgie en tête, utilisent toujours les phages en médecine traditionnelle, alors que les pays occidentaux les ont vite délaissés en raison de l’efficacité des antibiotiques, dont le spectre était plus large et la production en grandes quantités plus aisée et plus avantageuse économiquement. Aujourd’hui, la Belgique, la France ou les Etats-Unis s’y remettent doucement, convaincus que la phagothérapie constitue une alternative intéressante à creuser. Ainsi l’hôpital militaire Reine Astrid, à Neder-Over-Heembeek, s’y intéresse depuis longtemps. Il a développé une longue expertise. L’idée était de pouvoir utiliser les phages pour se protéger en cas de guerre bactériologique. Il continue de les cultiver et les livre gratuitement aux hôpitaux qui n’ont plus d’autres solutions pour sauver un patient. En Belgique, depuis 2008, une vingtaine de patients ont été traités par phagothérapie. Une start-up namuroise, Vésale Pharma, planche notamment sur un outil de diagnostic permettant de déterminer quels phages utiliser dans quel cocktail. Mais, pour l’instant, aucun grand laboratoire.
Sur le terrain, les acteurs évoluent dans un environnement peu favorable. Car les phages, issus du vivant, ne sont pas brevetables, contrairement aux antibiotiques. Des phages, il en existe en effet des milliards dans la nature, des déserts aux neiges éternelles en passant par notre tube digestif. A chaque fois, les équipes médicales doivent chercher le phage capable de canaliser une infection.
Stratégie 5 : le microbiote, un précieux allié
Les cent mille milliards de bactéries de notre organisme sont en effet la première barrière contre leurs homologues étrangères, pathogènes ou non. Elles les affament, produisent des antibiotiques naturels, et stimulent le système immunitaire. D’où la recherche de traitements pour protéger ou manipuler le microbiote contre les antibiotiques susceptibles de le mettre à mal, ou pour le reconstituer grâce à des » cocktails » de bactéries, comme les probiotiques qui, consommés en quantités adéquates, sont bénéfiques pour la santé de l’homme. D’autres pistes de protection du microbiote intestinal – administration d’un antibiotique conjointement à du charbon absorbant, ou à une bêta-lactamase agissant dans le côlon – sont à l’étude. A moins que l’on repeuple très rapidement la zone intestinale avec des bactéries inoffensives.
» C’est ce que l’on nomme la transplantation de flore, avec une réintroduction dans l’intestin de bactéries récupérées dans les selles d’un donneur sain ou même du patient avant le recours à l’antibiotique, puis mises en culture « , détaille Yves Van Laethem, évoquant plusieurs essais en ce sens, menés notamment en Belgique. Ce traitement fait désormais l’objet de recommandations internationales : plus de huit fois sur dix, il vient à bout de cette infection à Clostridium difficile, seule indication pour laquelle la greffe fécale est autorisée. Pour le reste, il s’agit d’essais cliniques incluant des patients qui ne répondent pas bien aux traitements classiques. Il reste toutefois encore difficile d’estimer l’impact que cela a, concrètement, en matière de lutte contre la prolifération de bactéries antibiorésistantes.